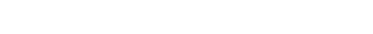当社の品質保証体制①
GMPについて
医薬品は、消費者の健康・生命に直接関わるもので、その品質は重要な項目となります。
医薬品の製造においては、GMP※「医薬品および医薬部外品の製造管理および品質管理に関する基準」として定められており、この基準に適合しなければ製造することはできません。
当社はGMPの3原則を遵守した製造管理、品質管理により、常に同じ品質、高い品質レベルでの医薬品製造に努めています。
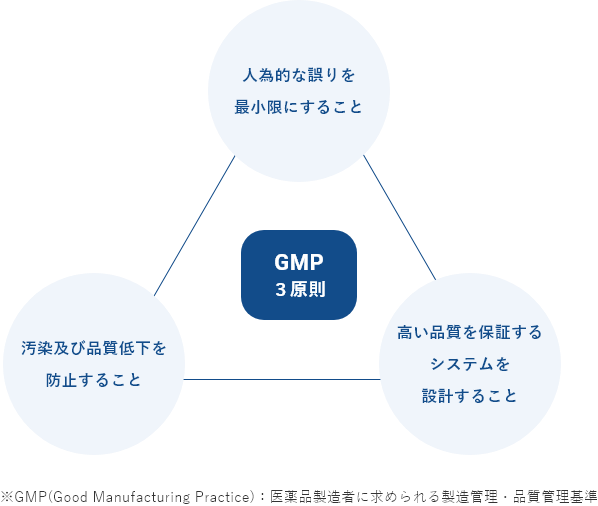
ダイトの品質保証体制
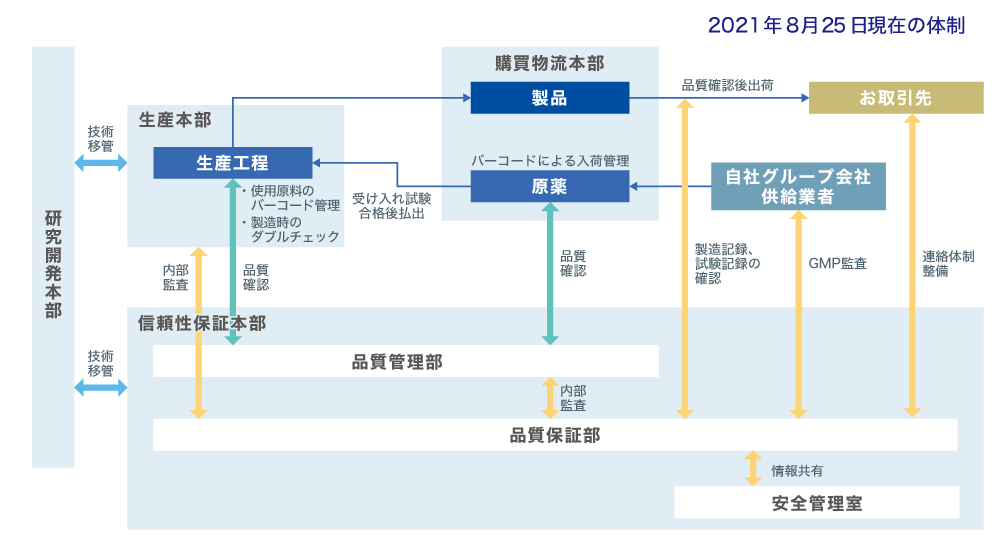
クオリティカルチャー(品質に関わる企業文化) を醸成することが、品質保証体制を支えます。
当社は1980年代より、品質を「競争力の源泉」と位置づけ、厚生労働省が定めるGMP(※)は元より、一般に国内よりもハードルが高いと言われるFDA(米国医薬食品局)の査察対応を進め、お取引先様、延いては患者様の信頼を得てきました。
当社の品質最優先の社風は、当時から変わることなく根付いており「ダイト 品質方針」に則り、安心して服用頂ける医薬品をご提供することを最優先事項として、事業活動を行っております。
(※ GMP : 医薬品及び医薬部外品の製造管理及び品質管理の基準)
また、これ以外にも、分析機器・製造機器に付属するコンピューターに関してGMP上必要とされる管理を行ったり(情報管理部門)、生産や品質管理を支える人員の採用や、社内へクオリティカルチャーの啓発活動を行う(総務人事部門)など、当社の品質保証体制は全社的な活動に支えられています。
当社の品質保証体制②
クオリティカルチャーの醸成
クオリティ・カルチャーとは
品質保証体制の土台にはクオリティ・カルチャー(品質文化)があります。当社では品質保証体制の充実のために、クオリティ・カルチャーの醸成にも注力しています。
クオリティカルチャーの基本的考え方
企業の品質分野で共有すべきクオリティカルチャーの要素とあるべき姿
信念
患者さんの生命を守ることを第一とする
価値観
経営層及び従業員が一体となり品質を優先するという意識
行動規範
安心して服用できる医薬品を安定的に供給するために、各従業員が品質確保の為自発的に行動し、判断するための実効性のある組織、システム、制度が構築され機能している
当社のクオリティ・カルチャー
当社では、1980年代より、品質を「競争力の源泉」と位置付け、業界では世界で最も厳しいと言われる米国当局(FDA)査察への対応を最重要課題として掲げ続けてきました。1989年より計11回(原薬・製剤 合計)のFDA査察実績を有し、長年にわたって、品質最優先の文化が浸透しております。
当社では、責任役員および関係部門長が、定期的に品質部門からの報告を受ける場 (品質マネジメントレビュー)を、少なくとも月に1回の頻度で開催しております。
多くの原薬・医薬品を製造していると、担当者のミスによって、市場に出荷できない製品が生産されてしまうことがあります。当社では、そのようなヒューマンエラーに対して「人は悪くない、しくみが悪い」という考え方に基づき、問題の根本的原因を見出し、その影響範囲全てについて「しくみ」で対処する文化が根付いています。
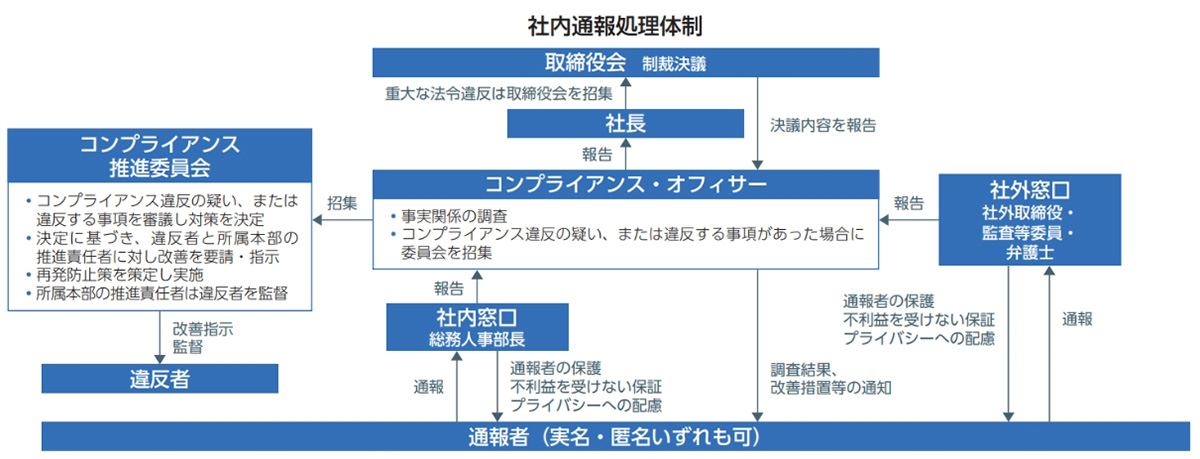
万が一、従業員が品質保証面で何らかの問題を発見し、それを指摘しても改善されない場合には、内部通報システムを利用して、社内や社外に設けられた相談窓口に直接、通報することが可能となっています。
ジェネリック医薬品の信頼性確保に関する対応
後発医薬品の製造販売承認書と製造・試験実態の整合性に関わる点検(2024年度)
製造販売承認書の再チェック(2021年度)
当社では、昨今の品質問題を極めて重要なことと受け止め、GE薬協会発第25号(令和3年3月25日付)に基づき、2021年3月より製造販売承認品目(全115品目)が承認書どおりに製造されているかどうかの再点検を行い、2021年11月に全品目の再点検が完了致しました。 その結果、重大な齟齬はございませんでした。

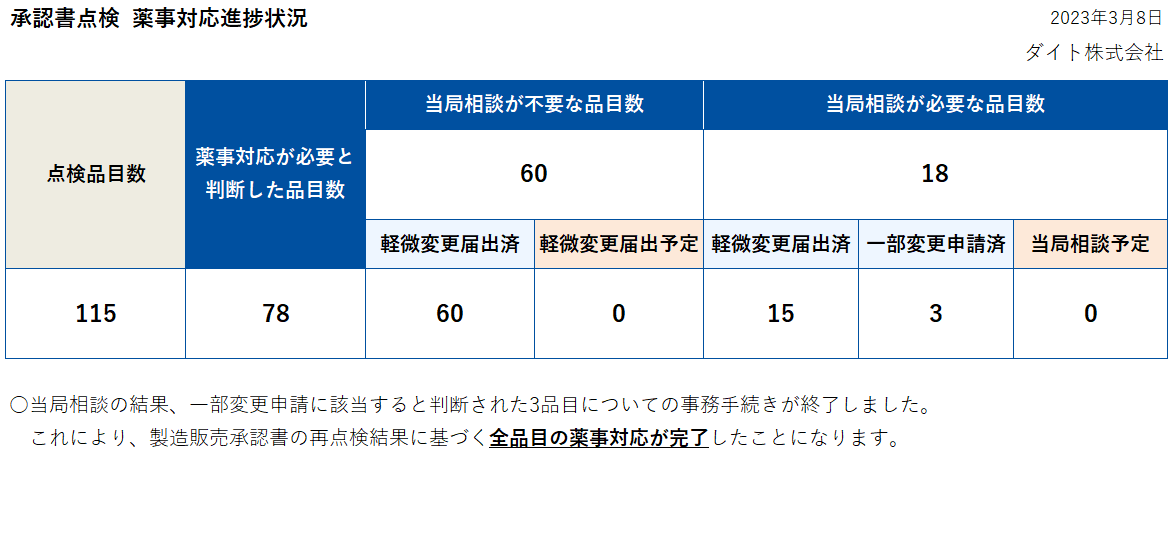
製造販売承認書の再点検結果に基づく行政対応について
当社の製造販売承認書に重大な齟齬はなかったものの品質に影響しない軽微な齟齬はございました。その対応として現在、承認書の手当てに伴う行政対応を順次進めております。
ダイトの医薬品に対する製造管理・品質管理の強化の取り組みについて
昨今のジェネリック業界における品質に係る問題に対して、当社の医薬品に対する製造管理・品質管理の強化の取り組みについてをお知らせいたします。